Er verschijnt zelden een molecuul dat de spelregels in de farmacologie zo drastisch herschrijft als retatrutide. Terwijl semaglutide en tirzepatide de afgelopen jaren de headlines domineerden, ontwikkelt Eli Lilly op de achtergrond een peptide dat niet op twee, maar op drie metabole receptoren tegelijk ingrijpt. De eerste fase 3-resultaten — gepubliceerd eind 2025 — bevestigen wat onderzoekers al vermoedden: retatrutide overtreft alles wat we tot nu toe kennen op het gebied van farmacologisch gewichtsverlies. In dit artikel nemen we de volledige werking, de klinische data, het doseerschema, de bijwerkingen en de toekomstverwachtingen onder de loep.
Hoe retatrutide werkt: drie receptoren, één injectie per week
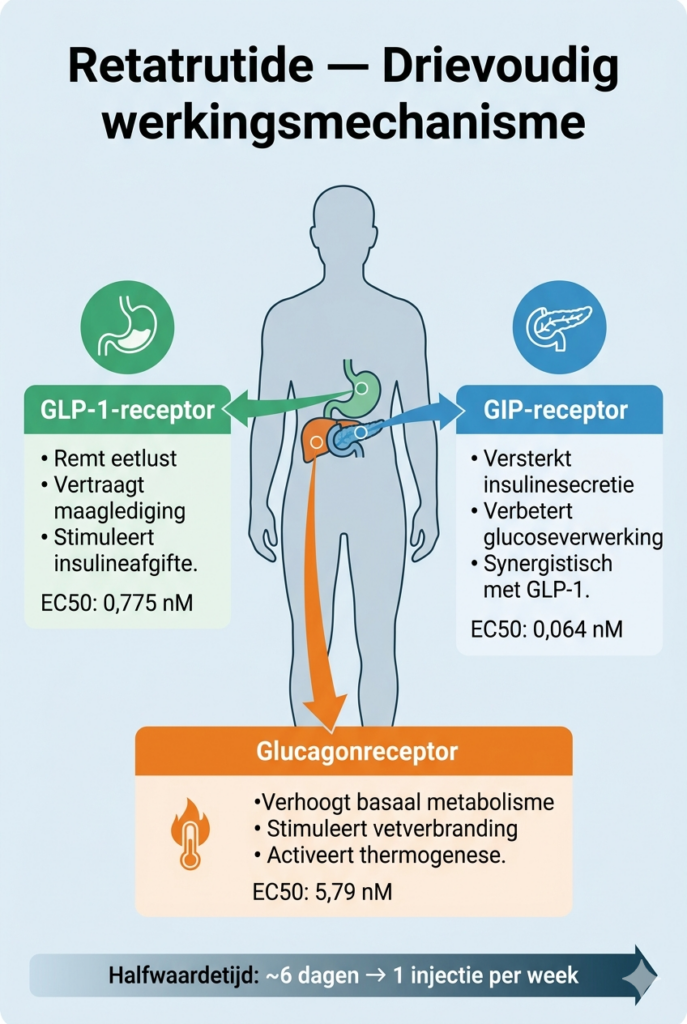
De kracht van retatrutide schuilt in het gelijktijdig activeren van drie hormoonreceptoren die elk een eigen rol spelen in de stofwisseling. We spreken over GLP-1 (glucagon-like peptide-1), GIP (glucose-dependent insulinotropic polypeptide) en de glucagonreceptor. Die combinatie maakt retatrutide uniek ten opzichte van elke andere behandeling die momenteel beschikbaar of in ontwikkeling is.
GLP-1, GIP en glucagon — wat doet elke receptor precies?
GLP-1-receptoractivatie kent iedereen inmiddels van semaglutide en liraglutide. Dit incretinehormoon remt de eetlust, vertraagt de maaglediging en stimuleert de insulineafgifte na een maaltijd. GIP versterkt dat effect: het bevordert de insulinesecretie en verbetert de manier waarop het lichaam glucose verwerkt. Tirzepatide combineert deze twee receptoren al met succes. Retatrutide voegt daar een derde dimensie aan toe — de glucagonreceptor. Glucagon is het tegenovergestelde van insuline: het verhoogt het basaal metabolisme, stimuleert de verbranding van vetzuren en activeert thermogenese in vetweefsel. In de praktijk betekent dit dat retatrutide niet alleen de voedselinname verlaagt (via GLP-1 en GIP), maar tegelijkertijd het energieverbruik verhoogt (via glucagon). Die combinatie verklaart waarom de gewichtsreductie in klinische studies zo consistent hoger uitvalt dan bij eerdere generaties medicijnen.
Uit moleculair onderzoek blijkt dat retatrutide de hoogste potentie vertoont op de GIP-receptor (EC50: 0,064 nM), gevolgd door de GLP-1-receptor (EC50: 0,775 nM) en de glucagonreceptor (EC50: 5,79 nM). De halfwaardetijd bedraagt ongeveer zes dagen, waardoor een wekelijkse subcutane injectie voldoende is om stabiele bloedspiegels te handhaven.
Klinische resultaten: van fase 2 naar fase 3
We hebben inmiddels data uit meerdere klinische trials — en de cijfers spreken voor zich. Retatrutide is niet zomaar een kleine verbetering ten opzichte van bestaande GLP-1-medicijnen; het vertegenwoordigt een categorieverschuiving.
Fase 2 — de studie die alles in gang zette
In de fase 2-trial, gepubliceerd in The New England Journal of Medicine (Jastreboff et al., 2023), werden 338 volwassenen met obesitas (BMI ≥ 30) zonder diabetes type 2 gerandomiseerd naar verschillende doseringen retatrutide of placebo, gedurende 48 weken. De resultaten lieten een duidelijk dosisafhankelijk patroon zien: bij de hoogste dosering van 12 mg per week bereikte het gemiddelde gewichtsverlies 24,2% van het startgewicht. Ter vergelijking: de placebogroep verloor slechts 2,1%.
Wat de data extra overtuigend maakt, is het percentage deelnemers dat klinisch relevante drempels haalde. Bij de 12 mg-groep bereikte 100% van de deelnemers minimaal 5% gewichtsverlies, 93% haalde de 10%-grens en 83% verloor 15% of meer van het startgewicht. Bij de 8 mg-groep waren deze percentages respectievelijk 100%, 91% en 75%. Zulke consistente responspercentages zijn ongekend in de geschiedenis van farmacologische obesitasbehandeling.
| Dosering | Gewichtsverlies (48 wk) | ≥5% verlies | ≥10% verlies | ≥15% verlies |
|---|---|---|---|---|
| Placebo | −2,1% | 27% | 9% | 2% |
| 1 mg/week | −8,7% | n.v.t. | n.v.t. | n.v.t. |
| 4 mg/week | −17,1% | 92% | 75% | 60% |
| 8 mg/week | −22,8% | 100% | 91% | 75% |
| 12 mg/week | −24,2% | 100% | 93% | 83% |
Parallel liep een fase 2-studie bij patiënten met diabetes type 2 (281 deelnemers). Na 36 weken daalde het HbA1c met 1,3 tot 2,0 procentpunt bij de hogere doseringen retatrutide, terwijl het gewichtsverlies in deze populatie gemiddeld rond de 17% lag bij de 12 mg-groep. Dat is opmerkelijk, omdat gewichtsverlies bij diabetespatiënten doorgaans moeilijker te realiseren is dan bij mensen zonder diabetes.
Fase 3 — TRIUMPH-4 en de bevestiging
In december 2025 publiceerde Eli Lilly de eerste fase 3-resultaten uit het TRIUMPH-programma. De TRIUMPH-4-trial onderzocht retatrutide bij 445 volwassenen met obesitas en knieartrose, zonder diabetes. Na 68 weken behandeling verloor de 12 mg-groep gemiddeld 28,7% van het lichaamsgewicht — omgerekend ruim 32 kilogram. Naast het gewichtsverlies daalden de pijnscores (gemeten via de WOMAC-schaal) met gemiddeld 4,5 punten, een reductie van bijna 76%. In een post-hocanalyse bleek dat circa 1 op de 8 behandelde deelnemers volledig pijnvrij was na 68 weken, tegenover 4,2% in de placebogroep.
Daarnaast verbeterde retatrutide meerdere cardiovasculaire risicofactoren. De systolische bloeddruk daalde bij de 12 mg-dosis met gemiddeld 14,0 mmHg, en er werden klinisch relevante reducties gemeten in non-HDL-cholesterol, triglyceriden en hooggevoelig C-reactief proteïne (hsCRP).
Het TRIUMPH-programma omvat in totaal acht fase 3-studies. Naast TRIUMPH-4 worden zeven extra trials verwacht in 2026, gericht op gewichtsbeheersing, diabetes type 2, obstructief slaapapneu, chronische lage rugpijn, leververvetting (MASLD) en cardiometabole uitkomsten. De breedte van dit onderzoeksprogramma weerspiegelt het vertrouwen dat Eli Lilly heeft in het molecuul — en de verwachting dat retatrutide goedkeuring kan krijgen voor meerdere indicaties tegelijk.
Retatrutide versus semaglutide en tirzepatide
De vraag die iedereen stelt: hoe verhoudt retatrutide zich tot de huidige topspelers op de markt? We hebben geen directe head-to-head-trials, maar de beschikbare data uit afzonderlijke studies laten een duidelijke rangorde zien.
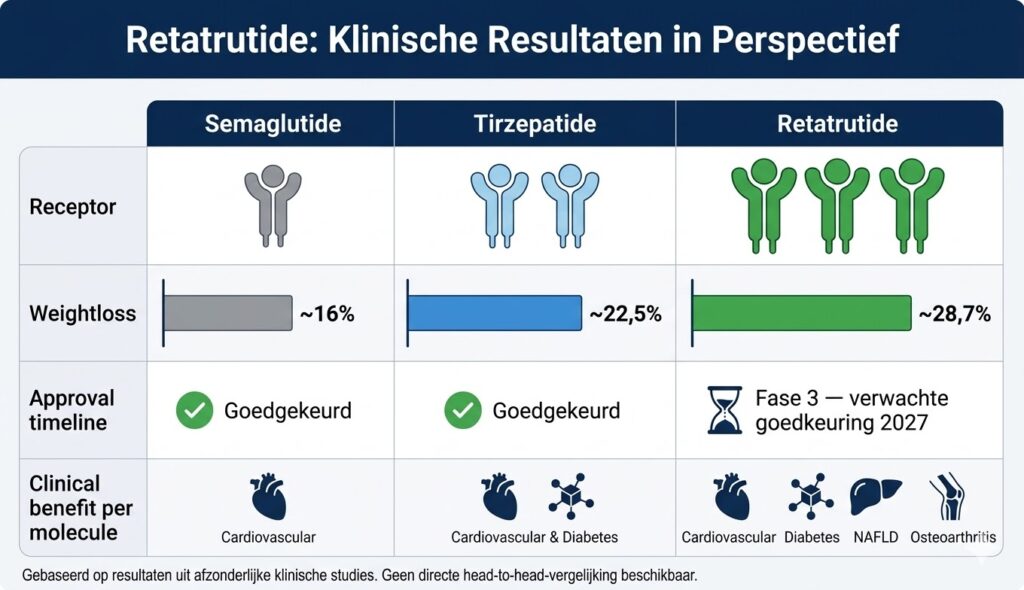
Semaglutide (het werkzame bestanddeel van Ozempic en Wegovy) is een enkelvoudige GLP-1-agonist. In de STEP-trials bereikte semaglutide 2,4 mg een gemiddeld gewichtsverlies van circa 15-17% na 68 weken. Tirzepatide (Mounjaro/Zepbound) is een duale GLP-1/GIP-agonist die in de SURMOUNT-1-trial bij de hoogste dosering van 15 mg een gewichtsverlies van ongeveer 22,5% realiseerde na 72 weken. Retatrutide overtreft beide: 24,2% na 48 weken in fase 2 en 28,7% na 68 weken in fase 3.
| Kenmerk | Semaglutide | Tirzepatide | Retatrutide |
|---|---|---|---|
| Receptoren | GLP-1 | GLP-1 + GIP | GLP-1 + GIP + glucagon |
| Type | Enkelvoudige agonist | Duale agonist | Tri-agonist |
| Max. gewichtsverlies | ~15-17% (68 wk) | ~22,5% (72 wk) | ~28,7% (68 wk) |
| Toediening | 1x per week, s.c. | 1x per week, s.c. | 1x per week, s.c. |
| Ontwikkelaar | Novo Nordisk | Eli Lilly | Eli Lilly |
| Status (maart 2026) | Goedgekeurd | Goedgekeurd | Fase 3 (TRIUMPH) |
| Effect op metabolisme | Eetlustremming | Eetlust + insuline | Eetlust + insuline + vetverbranding |
Het cruciale verschil zit in de glucagoncomponent. Waar semaglutide en tirzepatide voornamelijk de energie-inname verlagen, voegt retatrutide daar een actieve verhoging van het energieverbruik aan toe. In de praktijk betekent dit dat het lichaam niet alleen minder calorieën binnenkrijgt, maar ook efficiënter vet verbrandt — zelfs in rust. Die dubbele aanpak verklaart waarom retatrutide structureel hogere gewichtsverliescijfers laat zien dan zijn voorgangers.
We moeten hierbij wel kanttekeningen plaatsen. De vergelijkingen zijn indirect — verschillende studies hanteren verschillende populaties, behandelduren en eindpunten. Pas bij een directe head-to-head-trial kunnen we met zekerheid uitspraken doen over superioriteit. Maar de consistente trend is onmiskenbaar.
Doseerschema en opbouwprotocol
Een van de lessen uit de fase 2-data is dat de manier waarop retatrutide wordt opgebouwd een groot verschil maakt voor de verdraagbaarheid. Deelnemers die direct met een hogere startdosis begonnen, rapporteerden aanzienlijk meer maag-darmklachten dan degenen die geleidelijk werden opgebouwd.
Hoe ziet het opbouwschema eruit?
In de klinische trials startten deelnemers met 2 mg per week. Vervolgens werd de dosering elke vier weken verhoogd: van 2 mg naar 4 mg, dan naar 6 mg, vervolgens naar 9 mg en uiteindelijk naar 12 mg. Dit geleidelijke opbouwproces duurt circa 16 tot 20 weken voordat de onderhoudsdosering wordt bereikt. Die stapsgewijze benadering is niet willekeurig gekozen — het geeft het spijsverteringsstelsel de tijd om zich aan te passen aan de vertraagde maaglediging en de veranderde eetlustregulatie.
In de TRIUMPH-4-trial mochten deelnemers met hevige bijwerkingen de dosisverhoging uitstellen met twee tot vier weken zonder dat dit de uiteindelijke effectiviteit ondermijnde. Dat is een belangrijk gegeven: het toont aan dat individuele aanpassing van het opbouwschema mogelijk is zonder het eindresultaat in gevaar te brengen.
Het TRIUMPH-programma test daarnaast een onderhoudsdosis van 4 mg — naast de 9 mg en 12 mg uit TRIUMPH-4. De resultaten hiervan worden in 2026 verwacht en zullen helpen bepalen of lagere onderhoudsdoseringen voldoende zijn om het bereikte gewichtsverlies te behouden.
Bijwerkingen en veiligheidsprofiel
Geen enkel medicijn is vrij van bijwerkingen, en transparantie hierover is cruciaal. Het veiligheidsprofiel van retatrutide volgt grotendeels het patroon dat we kennen van andere incretinegebaseerde therapieën, met enkele belangrijke nuances.
Maag-darmklachten als meest voorkomende bijwerking
De meest gerapporteerde bijwerkingen zijn gastro-intestinaal van aard: misselijkheid, diarree, braken en constipatie. In de fase 2-studie werden deze klachten gemeld bij 35% van de deelnemers in de retatrutidegroepen — een percentage dat vergelijkbaar was met de actieve controlegroep (dulaglutide 1,5 mg). De klachten zijn dosisafhankelijk, treden vooral op tijdens de opbouwfase en zijn overwegend mild tot matig van ernst.
In de TRIUMPH-4-trial lagen de percentages hoger: misselijkheid bij 43% van de deelnemers, diarree bij 33% en braken bij 21%. We moeten deze cijfers in context plaatsen: de TRIUMPH-4-populatie bestond uit mensen met een gemiddeld startgewicht van 112,7 kg en een gemiddelde BMI van 40,4. Bij een dergelijke populatie en een behandelduur van 68 weken zijn hogere bijwerkingspercentages niet onverwacht.
Dysesthesie — een nieuw signaal
Een opvallende bevinding in TRIUMPH-4 was het optreden van dysesthesie — een abnormaal gevoel in de huid, zoals tintelingen, prikkelingen of een brandend gevoel. Dit bijwerking was niet eerder gemeld in de fase 2-trial en is daarom een punt van aandacht voor onderzoekers. Eli Lilly meldt dat de dysesthesiegevallen overwegend mild waren en zelden tot behandelstaking leidden. Analisten volgen dit signaal nauwlettend in de komende TRIUMPH-uitlezingen.
Behandelstaking en de context ervan
De stoppercentages door bijwerkingen bedroegen 12,2% bij 9 mg en 18,2% bij 12 mg, tegenover 4,0% bij placebo. Een deel van deze stakingen werd niet veroorzaakt door traditionele bijwerkingen, maar door wat Eli Lilly omschrijft als “waargenomen excessief gewichtsverlies.” Met andere woorden: sommige deelnemers stopten omdat zij sneller afvielen dan verwacht of gewenst. Bij deelnemers met een baseline BMI van 35 of hoger waren de stoppercentages aanzienlijk lager (8,8% bij 9 mg en 12,1% bij 12 mg), wat suggereert dat het middel juist bij hogere BMI-waarden goed wordt verdragen.
Extra metabole voordelen: lever, hart en gewrichten
Retatrutide laat effecten zien die verder reiken dan de weegschaal. Dat maakt het molecuul bijzonder interessant voor de bredere metabole gezondheidszorg.
Leververvetting (NAFLD/MASLD)
Een substudie binnen de fase 2-trial onderzocht het effect op leververvetting bij 98 patiënten met NAFLD. Na 48 weken behandeling met 8 of 12 mg retatrutide was bij meer dan 85% van de deelnemers de leversteatose volledig opgelost — gedefinieerd als een vetpercentage in de lever van minder dan 5% op MRI. Dit is een uitzonderlijk resultaat. Leververvetting treft naar schatting 25-30% van de volwassen bevolking en kan zonder behandeling evolueren naar leverfibrose en cirrose. De mogelijkheid dat retatrutide deze aandoening effectief aanpakt, opent een geheel nieuwe therapeutische dimensie.
Cardiovasculaire risicofactoren
In de TRIUMPH-4-trial verlaagde retatrutide non-HDL-cholesterol, triglyceriden en hsCRP — drie belangrijke voorspellers van cardiovasculair risico. De systolische bloeddrukdaling van 14 mmHg bij de 12 mg-dosis is klinisch zeer relevant; ter vergelijking, de meeste antihypertensiva bereiken een daling van 8-12 mmHg. Of deze verbeteringen zich vertalen naar een daadwerkelijke vermindering van hartinfarcten en beroertes, zal moeten blijken uit de lopende TRIUMPH-3-studie (cardiometabole uitkomsten).
Knieartrose en gewrichtsgezondheid
De TRIUMPH-4-resultaten tonen aan dat gewichtsverlies via retatrutide niet alleen de pijnscore bij knieartrose met 76% vermindert, maar ook de fysieke functie significant verbetert. Bij mensen met ernstig overgewicht draagt elke kilogram gewichtsverlies disproportioneel bij aan de verlichting van gewrichtsbelasting. Retatrutide zou in deze context een alternatief kunnen bieden voor patiënten die anders op een gewrichtsvervanging aansturen.
Wanneer wordt retatrutide beschikbaar?
De planning van Eli Lilly is ambitieus maar realistisch. Het TRIUMPH-programma omvat meer dan 5.800 deelnemers verspreid over acht fase 3-studies. De eerste succesvolle uitlezing (TRIUMPH-4) vond plaats in december 2025. Zeven aanvullende fase 3-uitlezingen worden verwacht in de loop van 2026. Op basis van deze tijdlijn projecteren analisten een mogelijke FDA-indiening eind 2026 en een potentiële goedkeuring in 2027. Voor de Europese markt (EMA-goedkeuring) kan daar nog zes tot twaalf maanden bij komen.
GlobalData schat de verwachte omzet van retatrutide op 15,6 miljard dollar in 2031. Die projectie weerspiegelt de verwachting dat retatrutide niet alleen concurreert met bestaande GLP-1-medicijnen, maar een aanzienlijk deel van de markt kan overnemen door zijn superieure effectiviteit. Eli Lilly investeert parallel in productiecapaciteit — een les die de farmaceutische industrie heeft geleerd van de tekorten bij semaglutide en tirzepatide.
Tot die tijd blijft retatrutide uitsluitend beschikbaar binnen klinische trials. Het is van groot belang om te benadrukken dat het kopen van retatrutide buiten goedgekeurde kanalen om risico’s met zich meebrengt. De FDA heeft reeds gewaarschuwd voor vervalste producten die online worden aangeboden. Zonder laboratoriumcertificering en zuiverheidsgarantie bestaat het risico op verontreinigingen, afwijkende doseringen of een verkeerde werkzame stof.
Wat retatrutide betekent voor de toekomst van gewichtsbeheersing
De opkomst van retatrutide markeert een verschuiving in hoe we naar obesitas kijken als medische aandoening. Waar de eerste GLP-1-agonisten bewezen dat farmacologisch gewichtsverlies van 10-15% haalbaar was, en tirzepatide die grens opschoof naar 20-22%, doorbreekt retatrutide consequent de 25%-barrière. Bij sommige deelnemers in de TRIUMPH-4-trial lag het gewichtsverlies boven de 30 of zelfs 35%.
Die omvang van gewichtsverlies was tot voor kort alleen bereikbaar via bariatrische chirurgie — een ingrijpende en onomkeerbare procedure. Retatrutide biedt voor het eerst een farmacologisch alternatief dat vergelijkbare resultaten levert, met het voordeel dat het omkeerbaar en doseerbaar is. Dat verandert het hele behandellandschap voor patiënten met ernstig overgewicht.
Toch blijven er open vragen. Wat gebeurt er als de behandeling wordt gestopt? Bij semaglutide en tirzepatide zien we dat een aanzienlijk deel van het gewicht terugkomt na het staken van de medicatie. Of retatrutide zich op dit punt onderscheidt, moet nog blijken uit langetermijndata. Daarnaast is de samenstelling van het gewichtsverlies relevant: hoeveel van de verloren kilogrammen bestaan uit vetmassa versus spiermassa? Uit studies met vergelijkbare incretinetherapieën komt naar voren dat 25-40% van het gewichtsverlies uit magere massa kan bestaan — een punt dat aandacht verdient, vooral bij langdurig gebruik.
De komende twaalf tot achttien maanden worden beslissend voor retatrutide. Met zeven fase 3-uitlezingen in het vooruitzicht, een mogelijke FDA-indiening en de eerste langetermijndata, zal 2026-2027 uitwijzen of de eerste resultaten standhouden in bredere populaties en over langere periodes. Voorlopig is de conclusie helder: retatrutide is het krachtigste gewichtsverliesmedicijn dat ooit in klinische trials is getest, en de implicaties daarvan reiken ver voorbij de weegschaal.





